|
||||
|
|
11. Азотсодержащие органические соединения 11.1. Нитросоединения. Амины Очень важны в народном хозяйстве азотсодержащие органические вещества. Азот может входить в органические соединения в виде нитрогруппы NO2, аминогруппы NH2 и амидогруппы (пептидной группы) – C(O)NH, причем всегда атом азота будет непосредственно связан с атомом углерода. Нитросоединения получают при прямом нитровании предельных углеводородов азотной кислотой (давление, температура) или при нитровании ароматических углеводородов азотной кислотой в присутствии серной кислоты, например: 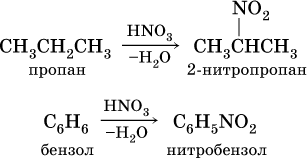 Низшие нитроалканы (бесцветные жидкости) используются как растворители пластмасс, целлюлозного волокна, многих лаков, низшие нитроарены (желтые жидкости) – как полупродукты для синтеза аминосоединений. Амины (или аминосоединения) можно рассматривать как органические производные аммиака. Амины могут быть первичными R – NH2, вторичными RR'NH и третичными RR'R" N, в зависимости от числа атомов водорода, которые замещены на радикалы R, R', R". Например, первичный амин — этиламин C2H5NH2, вторичный амин — дижетиламин (CH3)2NH, третичный амин – триэтиламин (C2H5)3N. Амины, как и аммиак, проявляют основные свойства, они в водном растворе гидратируются и диссоциируют как слабые основания: 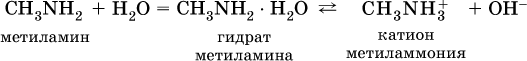 а с кислотами образуют соли: 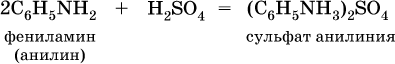 Третичные амины присоединяют галогенпроизводные с образованием солей четырехзамещенного аммония: 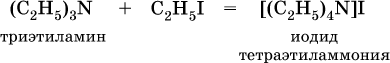 Ароматические ажины (в которых аминогруппа связана непосредственно с бензольным кольцом) являются более слабыми основаниями, чем алкиламины, из-за взаимодействия неподеленной пары электронов атома азота с ?-электронами бензольного кольца. Аминогруппа облегчает замещение водорода в бензольном кольце, например на бром; из анилина образуется 2,4,6-триброманилин: 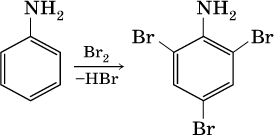 Получение: восстановление нитросоединений с помощью атомарного водорода (получают либо непосредственно в сосуде по реакции Fe + 2НCl = FeCl2 + 2Н0, либо при пропускании водорода Н2 над никелевым катализатором Н2 = 2Н0) приводит к синтезу первичных аминов: a) 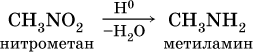 б) реакция Зинина 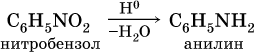 Амины используются в производстве растворителей для полимеров, лекарственных препаратов, кормовых добавок, удобрений, красителей. Очень ядовиты, особенно анилин (желто-коричневая жидкость, всасывается в организм даже через кожу). 11.2. Аминокислоты. Белки Аминокислоты – органические соединения, содержащие в своем составе две функциональные группы – кислотную СООН и аминную NH2; являются основой белковых веществ. Примеры:  Аминокислоты проявляют свойства и кислот, и аминов. Так, они образуют соли (за счет кислотных свойств карбоксильной группы): 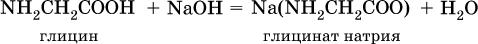 и сложные эфиры (подобно другим органическим кислотам): 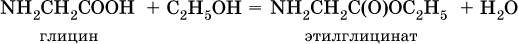 С более сильными (неорганическими) кислотами они проявляют свойства оснований и образуют соли за счет основных свойств аминогруппы: 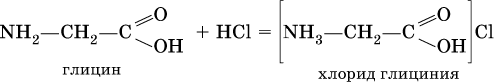 Реакцию образования глицинатов и солей глициния можно объяснить следующим образом. В водном растворе аминокислоты существуют в трех формах (на примере глицина): 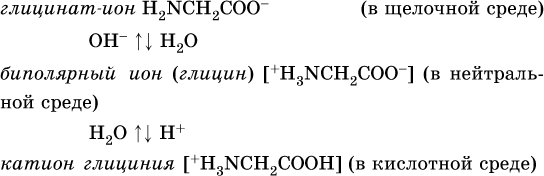 Поэтому глицин в реакции со щелочами переходит в глицинат-ион, а с кислотами – в катион глициния, равновесие смещается соответственно в сторону образования анионов или катионов. Белки – органические природные соединения; представляют собой биополимеры, построенные из остатков аминокислот. В молекулах белков азот присутствует в виде амидогруппы – С(О) – NH– (так называемая пептидная связь С – N). Белки обязательно содержат С, Н, N, О, почти всегда S, часто Р и др. При гидролизе белков получают смесь аминокислот, например: 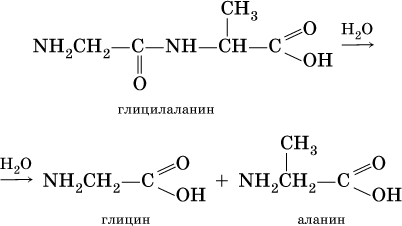 По числу остатков аминокислот в молекуле белка различают дипептиды (приведенный выше глицилаланин), трипептиды и т. д. Природные белки (протеины) содержат от 100 до 1 105 остатков аминокислот, что отвечает относительной молекулярной массе 1 • 104 – 1 • 107. Образование макромолекул протеинов (биополимеров), т. е. связывание молекул аминокислот в длинные цепи, происходит при участии группы СООН одной молекулы и группы NH2 другой молекулы: 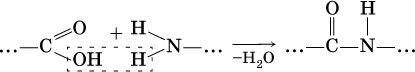 Физиологическое значение белков трудно переоценить, не случайно их называют «носителями жизни». Белки – основной материал, из которого построен живой организм, т. е. протоплазма каждой живой клетки. При биологическом синтезе белка в полипептидную цепь включаются остатки 20 аминокислот (в порядке, задаваемом генетическим кодом организма). Среди них есть и такие, которые не синтезируются вообще (или синтезируются в недостаточном количестве) самим организмом, они называются незаменимыми аминокислотами и вводятся в организм вместе с пищей. Пищевая ценность белков различна; животные белки, имеющие более высокое содержание незаменимых аминокислот, считаются для человека более важными, чем растительные белки. Примеры заданий частей А, В, С1—2. Класс органических веществ 1. нитросоединения 2. первичные амины содержит функциональную группу 1) – О – NO2 2) – NO2 3) – NH2 4) – NO3- 3. Водородные связи образуются между молекулами 1) формальдегида 2) пропанола-1 3) циановодорода 4) этиламина 4. Число структурных изомеров из группы предельных аминов для состава C3H9N равно 1) 1 2) 2 3) 3 4) 4 5. В водном растворе аминокислоты CH3CH(NH2)COOH химическая среда будет 1) кислотной 2) нейтральной 3) щелочной 4) любой 6. Двойственную функцию в реакциях выполняют (по отдельности) все вещества набора 1) глюкоза, этановая кислота, этиленгликоль 2) фруктоза, глицерин, этанол 3) глицин, глюкоза, метановая кислота 4) этилен, пропановая кислота, аланин 7—10. Для реакции в растворе между глицином и 7. гидроксидом натрия 8. метанолом 9. хлороводородом 10. аминоуксусной кислотой продуктами будут 1) соль и вода 2) соль 3) дипептид и вода 4) сложный эфир и вода 11. Соединение, которое реагирует с хлороводородом, образуя соль, вступает в реакции замещения и получается восстановлением продукта нитрования бензола, – это 1) нитробензол 2) метиламин 3) анилин 4) фенол 12. При добавлении лакмуса к бесцветному водному раствору 2-аминопропановой кислоты раствор окрашивается в цвет: 1) красный 2) желтый 3) синий 4) фиолетовый 13. Для распознавания изомеров со строением СН3—СН2—СН2—NO2 и NH2—СН(СН3) – СООН следует использовать реактив 1) пероксид водорода 2) бромная вода 3) раствор NaHCO3 4) раствор FeCl3 14. При действии концентрированной азотной кислоты на белок появляется… окрашивание: 1) фиолетовое 2) голубое 3) желтое 4) красное 15. Установите соответствие между названием соединения и классом, к которому оно относится  16. Анилин действует в процессах: 1) нейтрализация муравьиной кислотой 2) вытеснение водорода натрием 3) получение фенола 4) замещение с хлорной водой 17. Глицин участвует в реакциях 1) окисления с оксидом меди (II) 2) синтеза дипептида с фенилаланином 3) этерификации бутанолом-1 4) присоединения метиламина 18—21. Составьте уравнения реакций по схеме 18. 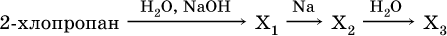 19. 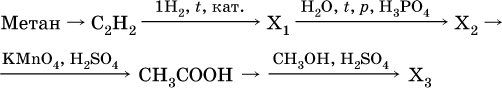 20. 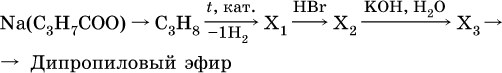 21.  |
|
||
