|
||||
|
|
Глава II. Тайна состава нефти и природных горючих газов
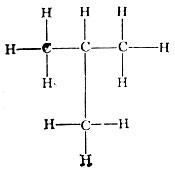
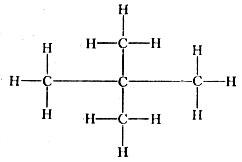
Тайна состава Слово "тайна" неоднократно встречается в этой книге, так как многое из того, что касается нефти и природных горючих газов, действительно, окружено тайной. В первую очередь это относится к составу нефти и природных горючих газов, который за 150 лет еще не окончательно изучен. Однако многое из того, что известно, тоже стало понятным не сразу, и потребовались усилия многих поколений исследователей, чтобы приблизиться к познанию состава нефтей и природных углеводородных газов. История раскрытия этой тайны тесно связана с историей развития химии вообще, а затем и органической химии и тоже полна догадок и заблуждений на пути к истине. Так, до начала XVIII века считалось, что нефть содержит горючее начало, которое связывали с наличием серы. Например, французский химик П. Ж. Макер (1718-1784 годы) считал, что нефть является лишь "одним родом" масел, которые "состоят из флогистона, соединенного с водой посредством кислоты и, кроме того, некоторого количества земли, различного в различных маслах". Однако уже в начале XIX века начали определять элементный состав нефти и природных газов сперва, конечно, не совсем точно, а затем удовлетворительно. Отнюдь не случайно Д. Дальтон апробировал Установленный им закон на примере состава метана и этилена и в 1808 году установил, что болотный газ имеет формулу СН2, а "маслородный" - СН. Пожалуй, именно с этого времени стало очевидным, что и нефть и сопровождавший ее природный газ состоят преимущественно из углеводородов. Однако, хотя авторы и указывали на непостоянство и сложность состава нефти, они даже отдаленно не могли представить действительную степень этой сложности; это касается и состава природных горючих газов. Но рассмотрим все по порядку. Родоначальник современной химии А. Л. Лавуазье (1743-1794 годы), который, по выражению Ф. Энгельса, "впервые поставил на ноги всю химию",[3] уже в то время понял, что органические вещества состоят из углерода и водорода и имеют гораздо более сложное строение, чем неорганические соединения, а Я. Берцелиус (1779-1848 годы) считал, что реакции между органическими соединениями не подчиняются установленным химическим законам, так как эти соединения обладают "жизненной силой". Господству этого представления пришел конец благодаря опытам Ф. Вёлера, который в 1828 году синтезировал мочевину. Это, собственно, и положило начало органической химии. В 1817 году французский химик X. Соссюр установил, что итальянская нефть содержит углеводороды (см. ниже), а английские химики в 1833 году пришли к выводу о том, что атомарное отношение углерода и водорода в нефтях подчиняется формуле СnН2n+2. Большое значение для понимания состава нефти имело установленное в 1843 году Ф. Жераром для органических соединений гомологических рядов. Для познания состава нефти много дали исследования Д, И. Менделеева, который в своем курсе "Органическая химия" указывал на наличие многих рядов углеводородов. Если в первой половине прошлого столетия состав нефти изучался в основном в познавательных целях и в учебных курсах углеводороды рассматривались просто как группа соединений (например "углеродистые во-дороды" в упомянутом курсе Д. И. Менделеева), то с 50-60-х годов XIX столетия углеводороды нефтей (в России кавказских, в США пенсильванских) начала изучать как промышленное сырье. В 1934 году В. Трайбс открыл в нефти металлоорганические азотистые соединения - порфирины, являющиеся производными хлорофилла и гемоглобина. Но наиболее значительная часть современной информации о составе нефти была получена в последние десятилетия. Остановимся сначала на общей характеристике нефти и природных углеводородных газов. Начнем с нефти. По физическим свойствам ее можно назвать парадоксом земной коры: в мощной толще горных пород, пропитанных водой и содержащих ее в самых различных состояниях, вдруг появляется вещество, по всем своим свойствам противоположное воде, "не любящее" ее - гидрофобное, плотность которого всегда меньше плотности воды и в отличие от нее не повышается с глубиной, а, как правило, понижается. Если вода стремится занять в породах в первую очередь самые мелкие поры и трещины, то нефть, наоборот, - самые крупные. Нефть представляет собой жидкость, чаще всего коричневую, с зеленоватым или другими оттенками, иногда почти черную и очень редко бесцветную. Нефть всегда легче воды, ее плотность изменяется в широких пределах от 0,76 до 0,99 г/см3, чаще всего составляя 0,80-0,87 г/см3. Очень редко, но в значительных количествах встречается нефть с такой же, как у воды, плотностью - 1,0 г/см3 и даже более тяжелая, чем вода - 1,03-1,04 г/см3 (месторождение Окснард в Калифорнии). В соответствии с плотностью, как правило, меняется и вязкость нефти от 1,41 до 660 мПа?с: легкие нефти обычно маловязкие, средние по плотности нефти - вязкие и очень вязкие и, наконец, существуют полутвердые нефти (например, в песчаниках Ярегского месторождения на Ухте). Плотность и вязкость нефти зависят от многих факторов, в первую очередь от температуры и количества растворенных в нефти газов. Поверхностное натяжение у нефти (17-28 дин/см2) почти в 3 раза меньше, чем у воды (75 дин/см2), вследствие чего вода всегда вытесняет нефть из мелких пор в крупные. Температура кипения нефти колеблется в широких пределах - от 70 до 250 °С. Одной из примечательных особенностей нефти является ее способность растворять огромное количество углеводородных газов - до 400 м3 в 1 м3 нефти (в зависимости от состава нефти и газа, величин давления и температуры) и самой растворяться в них (обратная, ретроградная растворимость) - до 400 г нефти в 1 м3 газа. При этом чем больше в нефти растворено газа, тем меньше ее плотность и вязкость. Использование нефти в качестве энергетического сырья связано с ее максимальной для минеральных топлив теплотворной способностью 42 тыс. кДж/кг. Для сравнения отметим, что теплотворная способность (в кДж/кг) составляет: торфа - 10 500-14 700, каменного угля - 21 000-30 240, антрацита - 27 300-31 500. Нефть обладает рядом интересных оптических свойств: она может люминесцировать - светиться под ультрафиолетовыми лучами, вращать плоскость поляризации светового луча и т.д. Молекулярный вес нефти обычно колеблется в пределах 240-290, иногда превышая эту величину. Изменение всех физических свойств нефтей связано с изменением их химического состава. Из каких же элементов состоит нефть? Главным ее компонентом является углерод, составляющий от 83 до 87% нефти. Второе место занимает водород, содержание которого обычно колеблется в пределах 12-14%. Третье место в составе нефти принадлежит группе так называемых гетероэлементов: кислорода, азота и серы, суммарное содержание которых может достигать 5-8%, но обычно бывает меньше. В нефти в весьма небольших количествах встречаются фосфор, ванадий, никель, железо, алюминий, кальций, магний, барий, стронций, марганец, хром, кобальт, молибден, бор и другие элементы (всего 44). Серу и различные элементы, содержащиеся в нефти, можно извлекать, в связи с чем нефть следует рассматривать не только в качестве энергетического сырья, но и как сырье для получения этих элементов. В нефти и горючих газах углерод и водород содержатся в виде удивительнейших и огромнейших групп соединений - углеводородов, отличающихся исключительным разнообразием, изменчивостью состава и строения и широким распространением, особенно в растительных и животных организмах. По соотношению углерода и водорода углеводороды дифференцируются на три большие группы: 1) парафиновые, или насыщенные, в химии чаще всего выделяемые под названием алканов; 2) нафтеновые, или полиметиленовые, и 3) ароматические (арены). Парафиновые углеводороды имеют общую формулу CnH2n+2. Первые члены этой группы - газы: метан - СН4, этан - С2Н6, пропан - С3Н8 и бутан - С4Н10. Углеводороды с числом углеводородных атомов от 5 до 15 - жидкие, а с более высоким числом - твердые. Мало того, алканы одного и того же состава могут иметь молекулы нормального строения и изостроения, разветвленные. Благодаря этому, начиная с бутана, наряду с углеводородами нормального строения имеются углеводороды изостроения, причем число изомеров растет одновременно с числом углеродных атомов: у пентана два изомера, у гексана четыре, у октана 17, углеводорода O2H26 имеет более 300 изомеров, углеводород C13H28 - 800 изомеров и т. д.
Изобутан (СН3)2СН?СН3; точка кипения - 10,2°С
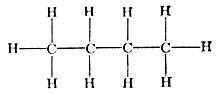
н - бутан СН3(СН2)2СН3; точка кипения - 0,5°С
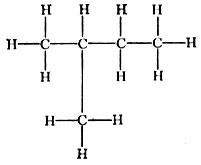
Изопентан CH (СН3)2СH2СН3; точка кипения 28°С
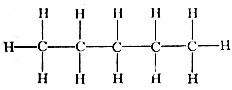
н - центам СН3(СН2)3СН3: точка кипения 36°С
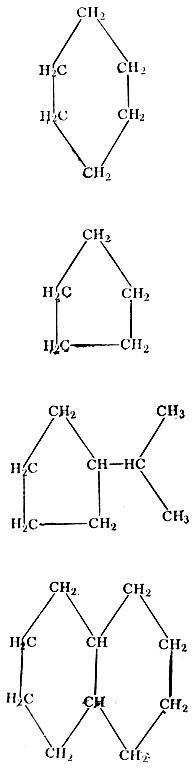
Третичный пентан, неопентан, тетраметилметан или 2,2-димстилпропа:' С(СН3)4 Точка кипения 9,45°С Нафтеновые углеводороду, содержащиеся в нефти, имеют циклическое строение. Поэтому их иногда называют цикланами или насыщенными циклическими СnН2n. Циклы состоят из пяти (циклопентан) или шести (циклогексан) атомов углерода. При этом таких циклов бывает несколько, в связи с чем к названию добавляется приставка моно-, би-, три- или тетра-.
Циклическое строение Кроме того, циклы имеют еще и боковые цепи. В этой группе, начиная с углеводорода С4Н8, встречаются изомеры, число которых также увеличивается с возрастанием числа углеродных атомов: у C6H12 - 13 изомеров, у C7H14 - 27 изомеров и т. д.
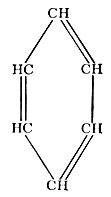
Боковые цепи Ароматические углеводороды, имеющие общую формулу СnН2n-6, обычно содержатся в нефти в меньших количествах, чем углеводороды двух описанных выше групп. Они также имеют преимущественно циклическое строение, но между отдельными атомами углерода в них в отличие от нафтенов наряду с одинарными связями имеются и двойные.
Бензол
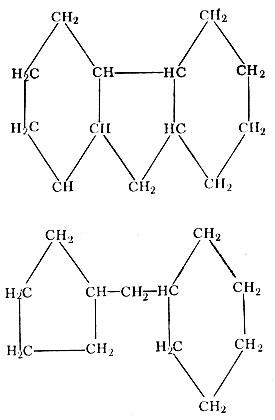
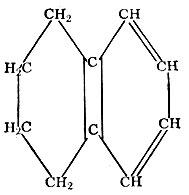
Тетралин
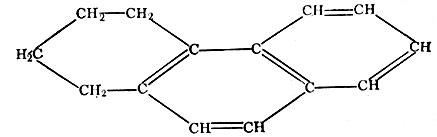
Тетрагидрофенантрен Кроме того, в отдельных группах водород замещается метильной группой СН3. Ароматические углеводороды нефти могут содержать один, два и более циклов и соответственно называются моно-, би-, три- и тетра-циклическими. Наконец, еще в нефти содержатся нафтеново-ароматические углеводороды.
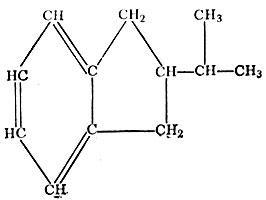
Нафтеново-ароматические углеводороды Всего в нефти к настоящему времени определено 425 индивидуальных углеводородов, в действительность же их значительно больше. Гетероэлементы (сера, азот и кислород) обычно содержатся в нефти в виде сложных соединений, ядрами которых являются углеводороды, и значительно реже - в чистом виде. Общее число определенных гетеросоединений превышает 380, из них сернистых 250. Кроме того, в строении сложных органических соединений участвуют фосфор, уран, ванадий, никель, кобальт, иод, бор и другие элементы. Существенную часть в нефти составляют смолы и асфальтены, химическая природа которых достаточно точно не определена. При этом чем тяжелее нефть, тем выше ее плотность и тем больше она содержит смол асфальтенов. В нефти содержатся еще и металлоорганические комплексы, представляющие собой по строению сложные полициклические углеводороды, в молекуле которых отдельные атомы водорода или метальные группы замещены атомами металлов. Среди них особое значение, как отмечалось, имеют порфирины, являющиеся производными хлорофилла и гемоглобина. Всего в нефти индентифицировано более 900 индивидуальных химических соединений, причем ни в одном из ее образцов не определены полностью все имеющиеся в нем индивидуальные соединения. К настоящему времени удалось изучить распределение в нефти изотопов некоторых элементов - углерода, серы и водорода (табл. 1). Как известно, изотопами называются атомы, имеющие одинаковые количества протонов, но разное количество нейтронов (N) и, как следствие этого, обладающие разным массовым числом (А) или атомной массой. < border="0"> Таблица 1. Некоторые сведения об изотопах водорода, углерода и серы Z Элемент N A Относительная распространенность ат. % 1 Водород Н 0 1 99,9844 1 Дейтерий Д 1 2 0,0156 1 Тритий Т 2 3 - 6 Углерод С 6 12 98,892 6 Углерод С 7 13 1,108 6 Углерод С 8 14 - 16 Сера S 16 32 95,1 16 Сера S 17 33 0,74 16 Сера S 18 34 4,2 16 Сера S 20 36 0,016 Изотопы делятся на стабильные и радиоактивные. Последние самопроизвольно распадаются. Так, изотоп углерода 14С является радиоактивным и период его полураспада составляет 5568 лет. Благодаря этим свойствам оказалось возможным определять по содержанию 14С возраст многих археологических объектов и геологических образований не древнее 30 000 лет. Содержание стабильных изотопов углерода, серы и водорода в нефти разных регионов мира и в разных породах изучено не одинаково. Теперь о газах. Горючие углеводородные газы, бесцветные, почти в 2 раза легче воздуха. Они, как правило, не имеют запаха, однако при наличии примеси сероводорода, приобретают неприятный запах и становятся очень токсичными. Теплотворная способность газов составляет 27 300-37 800 кДж/м3, а попутных газов из нефтяных месторождений достигает 42 000-71 400 кДж/м3. Основным компонентом природных горючих газов является метан, количество которого может достигать 99,5%, но обычно колеблется в пределах 85-95%. В газах довольно часто содержатся и гомологи метана - этан, пропан и бутан, а также их изомеры - изопропан и изобутан. Как правило, газы в нефтяных залежах обогащены гомологами метана, содержание которых обычно составляет 10-15%, но иногда достигаем и 50-60% (месторождения Ромашкино, Мухановс и др.). Эти примеси в газе представляют самостоятельный интерес как сырье для производства многих материалов (полиэтилена и др.), тем самым позволяя экономить нефть. Среди неуглеводородных компонентов в составе природных газов наиболее часто встречается азот, содержание которого может достигать 90-95%, вплоть для перехода газа в чисто азотный. В весьма широких пределах колеблется в природных газах содержание двуокиси углерода - от долей процента до 95% (как, например, в месторождениях Калифорнии, Мексики и др.) Довольно часто в состав природных горючих газов 1зных количествах входит сероводород: например, в газax Оренбургского месторождения его содержание достигает 15%, а в газах Астраханского - 23%. Встречаются газы, содержащие более 50% сероводорода. Сероводород в природном газе одновременно и "добро" и зло". При очистке такого газа получают большие количества серы, столь необходимой промышленности и сельскому хозяйству (например, на Оренбургском газоконденсатном месторождении). В ближайшем будущем предусмотрено и освоение Астраханского газоконденсатного месторождения. В то же время сероводород токсичен и агрессивен по отношению к металлам, вследствие чего все оборудование, начиная от труб в скважинах, должно быть изготовлено из специальных сталей. В природных горючих газах обычно содержатся гелий и в значительно меньших количествах аргон, неон, ксенон и другие инертные газы. В последние десятилетия обнаружены газоконденсаты, которые находятся в газовых залежах в газообразном состоянии (от 1 до 1000 г в 1 м3), а на поверхности при снижении температуры и давления переходят в жидкость. Газоконденсаты представляют собой бесцветные или светло-коричневые жидкости, плотностью от 0,66 до 0,84 г/см3 (чаще 0,72-0,80 г/см3), характеризующиеся низкими температурами кипения (30- 70 °С) и почти полностью выкипающие при температуре до 300-350 °С. Газоконденсаты состоят преимущественно из углеводородов, среди которых чаще преобладают метановые, но иногда и нафтеновые и ароматические разности. В конденсатах нередко содержится сера, реже - смола. Углеводороды содержатся в составе органического вещества горных пород, подземных водах, а также в современных осадках и водах земной поверхности, и многих веществ растительного и животного происхождения. Углеводородные газы находятся не только в сообщающихся пустотных пространствах горных пород (в случае образования залежей), но и в закрытых порах, также в сорбированном минеральной частью виде, часто вблизи мест своего "рождения" и растворены в подземных водах. Примечания:3 Маркс К., Энгельс Ф. Соч., 2-е изд., т. 24, с. 20. |
|
||