|
||||
|
|
Лекция № 16. Инфузионная терапия Инфузионная терапия – это капельное введение или вливание внутривенно или под кожу лекарственных средств и биологических жидкостей с целью нормализации водно-электролитного, кислотно-щелочного баланса организма, а также для форсированного диуреза (в сочетании с мочегонными средствами). Показания к инфузионной терапии: все разновидности шока, кровопотери, гиповолемия, потеря жидкости, электролитов и белков в результате неукротимой рвоты, интенсивного поноса, отказа от приема жидкости, ожогов, заболеваний почек; нарушения содержания основных ионов (натрия, калия, хлора и др.), ацидоз, алкалоз и отравления. Главные признаки обезвоживания организма: западение глазных яблок в орбиты, тусклая роговица, кожные покровы сухие, неэластичные, характерно сердцебиение, олигурия, моча становится концентрированной и темно-желтой, общее состояние угнетенное. Противопоказаниями к инфузионной терапии являются острая сердечно-сосудистая недостаточность, отек легких и анурия. Кристаллоидные растворы способны восполнять дефицит воды и электролитов. Применяют 0,85 %-ный раствор натрия хлорида, растворы Рингера и Рингера—Локка, 5 %-ный раствор натрия хлорида, 5—40 %-ные растворы глюкозы и другие растворы. Их вводят внутривенно и подкожно, струйно (при выраженном обезвоживании) и капельно, в объеме 10–50 и более мл/кг. Эти растворы не вызывают осложнений, за исключением передозировки. Цели инфузионной терапии: восстановление ОЦК, устранение гиповолемии, обеспечение адекватного сердечного выброса, сохранение и восстановление нормальной осмолярности плазмы, обеспечение адекватной микроциркуляции, предупреждение агрегации форменных элементов крови, нормализация кислородно-транспортной функции крови. Коллоидные растворы – это растворы высокомолекулярных веществ. Они способствуют удержанию жидкости в сосудистом русле. Используют гемодез, полиглюкин, реополиглюкин, реоглюман. При их введении возможны осложнения, которые проявляются в виде аллергической или пирогенной реакции. Пути введения – внутривенно, реже подкожно и капельно. Суточная доза не превышает 30–40 мл/кг. Обладают дезинтоксикационным качеством. Как источник парентерального питания применяются в случае длительного отказа от приема пищи или невозможности кормления через рот. Применяют гидролизины крови и казеина (альвезин-нео, полиамин, липофундин и др.). Они содержат аминокислоты, липиды и глюкозу. Иногда на введение бывает аллергическая реакция. Темп и объем инфузии. Все инфузии с позиции объемной скорости вливания можно разграничить по двум категориям: требующие и не требующие быстрой коррекции дефицита ОЦК. Основную проблему могут представлять больные, которые нуждаются в быстрой ликвидации гиповолемии. т. е. темп проводимой инфузии и ее объем должны обеспечивать производительность сердца, чтобы должным образом снабдить регионарную перфузию органов и тканей без значительной централизации кровообращения. У пациентов с исходно здоровым сердцем максимально информативны три клинических ориентира: среднее АД > 60 мм рт. ст.; центральное венозное давление – ЦВД > 2 см вод. ст.; диурез 50 мл/ч. В сомнительных случаях проводят пробу с нагрузкой в объеме: в течение 15–20 мин вливают 400–500 мл кристаллоидного раствора и наблюдают за динамикой ЦВД и диуреза. Значительный подъем ЦВД без увеличения диуреза может указывать на сердечную недостаточность, что подсказывает необходимость провести более сложные и информативные методы оценки гемодинамики. Сохранение обоих показателей низкими говорит о гиповолемии, тогда поддерживают высокую скорость вливаний с повторной поэтапной оценкой. Увеличение диуреза обозначает преренальную олигурию (гипоперфузию почек гиповолемического генеза). Инфузионная терапия у пациентов с недостаточностью кровообращения требует четких знаний гемодинамики, большого и специального мониторного наблюдения. Декстраны – это коллоидные плазмозаменители, что обуславливает их высокую эффективность в быстром восстановлении ОЦК. Декстраны имеют специфические защитные свойства в отношении ишемических заболеваний и реперфузии, риск которых всегда присутствует при проведении больших хирургических вмешательств. К отрицательным сторонам декстранов следует отнести риск развития кровотечений за счет дезагрегации тромбоцитов (особенно характерно для реополиглюкина), когда возникает необходимость использования значительных доз препарата (> 20 мл/кг), и временное изменение антигенных свойств крови. Декстраны опасны способностью вызывать «ожог» эпителия канальцев почек и поэтому противопоказаны при ишемии почек и почечной недостаточности. Они часто вызывают анафилактические реакции, которые бывают весьма тяжелыми. Особый интерес представляет раствор человеческого альбумина, так как является природным коллоидом плазмозаменителя. При многих критических состояниях, сопровождающихся повреждением эндотелия (прежде всего при всех видах системных воспалительных заболеваний) альбумин способен переходить в межклеточное пространство внесосудистого русла, притягивая к себе воду и ухудшая интерстициальный отек тканей, в первую очередь легких. Свежезамороженная плазма – это продукт, взятый от одного донора. СЗП отделяется от цельной крови и немедленно замораживается в течение 6 ч после забора крови. Хранится при температуре 30 °C в пластиковых пакетах в течение 1 года. Учитывая лабильность факторов свертывания, СЗП должна быть перелита в течение первых 2 ч после быстрой разморозки при температуре 37 °C. Переливание свежезамороженной плазмы (СЗП) дает высокий риск заражения опасными инфекциями, такими как ВИЧ, гепатиты В и С и др. Частота анафилактических и пирогенных реакций при переливании СЗП весьма высока, поэтому совместимость по системе АВО должна учитываться. А для молодых женщин необходимо учитывать Rh-совместимость. В настоящее время единственным абсолютным показанием к применению СЗП является профилактика и лечение коагулопатических кровотечений. СЗП выполняет сразу две важнейшие функции – гемостатическую и поддержания онкотического давления. СЗП также переливают при гипокоагуляции, при передозировке непрямыми антикоагулянтами, при проведении лечебного плазмофереза, при остром ДВС-синдроме и при наследственных заболеваниях, связанных с дефицитом факторов свертывания крови. Показателями адекватной проводимой терапии являются ясное сознание больного, теплые кожные покровы, стабильная гемодинамика, отсутствие выраженной тахикардии и одышки, достаточный диурез – в пределах 30–40 мл/ч. 1. Гемотрансфузия Осложнения гемотрансфузии: посттрансфузионные расстройства системы свертывания крови, тяжелые пирогенные реакции с наличием гипертермического синдрома и сердечно-сосудистой декомпенсацией, анафилактические реакции, гемолиз эритроцитов, острая почечная недостаточность и т. д. В основе большинства осложнений лежит реакция отторжения организмом чужеродной ткани. Показаний к переливанию цельной консервированной крови нет, потому что значителен риск посттрансфузионных реакций и осложнений, но наиболее опасным является высокий риск заражения реципиента. При острой кровопотере при хирургическом вмешательстве и адекватном восполнении дефицита ОЦК даже резкое снижение гемоглобина и гематокрита не угрожает жизни больного, так как потребление кислорода под наркозом значительно уменьшается, допустима дополнительная оксигенация, гемодилюция способствует профилактике возникновения микротромбообразования и мобилизации эритроцитов из депо, увеличению скорости кровотока и т. д. Имеющиеся у человека от природы «запасы» эритроцитов значительно превышают реальные потребности, тем более в состоянии покоя, в котором в это время находится пациент. Рекомендации по назначению переливания донорской крови и эритроцитов во время операции. 1. Переливание эритроцитарной массы проводится после восстановления ОЦК. 2. При наличии тяжелой сопутствующей патологии, которая может привести к летальному исходу (например, при тяжелой ишемической болезни сердца плохо переносится выраженная анемия). 3. При наличии следующих показателей красной крови больного: 70–80 г/л для гемоглобина и 25 % для гематокрита, а количество эритроцитов 2,5 млн. Показанием к переливанию крови являются: кровотечение и коррекция гемостаза. Виды эритросред: цельная кровь, эритроцитарная масса, ЭМОЛТ (эритроцитарная масса, отделенная от лейкоцитов, тромбоцитов с физиологическим раствором). Кровь вводят внутривенно капельно, при помощи одноразовой системы при скорости 60– 100 капель в минуту, в объеме 30–50 мл/кг. Перед переливанием крови обязательно проводится определение группы крови и резус-фактора реципиента и донора, проводят пробу на их совместимость, а у постели больного проводится биологическая проба на совместимость. При появлении анафилактической реакции трансфузия прекращается и начинаются мероприятия по ликвидации шока. Концентрат тромбоцитов стандартный – это суспензия дважды отцентрифугированных тромбоцитов. Минимальное количество тромбоцитов 0,5 ? 1012 на литр, лейкоцитов – 0,2 ? 109 на литр. Гемостатические характеристики и выживание наиболее выражены в ближайшие 12–24 ч приготовления, но препарат может быть использован в течение 3–5 дней с момента забора крови. Концентрат тромбоцитов используется при тромбоцитопении (лейкемия, аплазия костного мозга), при тромбопатии с геморрагическим синдромом. 2. Парентеральное питание При тяжелых заболеваниях, сопровождающихся выраженными нарушениями гомеостаза, необходимо обеспечить организм энергетическим и пластическим материалом. Поэтому, когда питание через рот по каким-либо причинам нарушено или совсем невозможно, необходимо переводить больного на парентеральное питание. При критических состояниях различной этиологии самые значительные изменения происходят в метаболизме белков – наблюдается интенсивный протеолиз, особенно в поперечнополосатой мускулатуре. В зависимости от тяжести протекающего процесса белки организма катаболизируются в количестве 75—150 г в сутки (суточные потери белка приведены в таблице 11). Это ведет к дефициту незаменимых аминокислот, которые используются в качестве источника энергии в процессе гликонеогенеза, что приводит к отрицательному азотистому балансу. Таблица 11 Суточные потери белка в критических состояниях 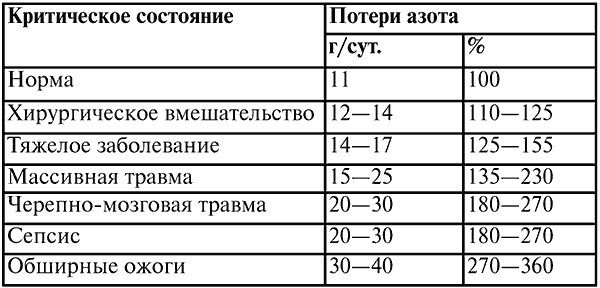 Потеря азота приводит к уменьшению массы тела, так как: 1 г азота = 6,25 г белка (аминокислот) = 25 г мышечной ткани. Уже через сутки от начала критического состояния без адекватной терапии с введением достаточного количества основных питательных веществ исчерпываются собственные запасы углеводов, и организм получает энергию от белков и жиров. В связи с этим осуществляются не только количественные, но и качественные изменения метаболических процессов. Основными показаниями для проведения парентерального питания являются: 1) аномалии развития желудочно-кишечного тракта (атрезия пищевода, стеноз привратника и другие, пред– и послеоперационный период); 2) ожоги и травмы ротовой полости и глотки; 3) обширные ожоги тела; 4) перитонит; 5) паралитическая непроходимость кишечника; 6) высокие кишечные свищи; 7) неукротимая рвота; 8) коматозное состояние; 9) тяжелые заболевания, сопровождающиеся усилением катаболических процессов и декомпенсированными нарушениями метаболизма (сепсис, тяжелые формы пневмонии); 10)атрофия и дистрофия; 11) анорексия в связи с неврозами. Парентеральное питание должно проводиться в условиях компенсации волемических, водно-электролитных нарушений, ликвидации расстройств микроциркуляции, гипоксемии, метаболического ацидоза. Основной принцип парентерального питания – обеспечение организма адекватным количеством энергии и белка. С целью парентерального питания применяют следующие растворы. Углеводы: наиболее приемлемым препаратом, применяемым в любом возрасте, является глюкоза. Соотношение углеводов в суточном рационе должно быть не менее 50–60 %. Для полной утилизации требуется выдержать скорость введения, снабжать глюкозу следует ингредиентами – инсулин 1 ЕД на 4 г, калий, коферменты, участвующие в утилизации энергии: пиридоксальфосфат, кокарбоксилаза, липоевая кислота, а также АТФ – 0,5–1 мг/кг в сутки внутривенно. При правильном введении высококонцентрированная глюкоза не вызывает осмотического диуреза и значительного повышения уровня сахара крови. Для проведения азотистого питания применяют либо высококачественные белковые гидролизаты (аминозол, аминон), либо растворы кристаллических аминокислот. В этих препаратах удачно сочетаются незаменимые и заменимые аминокислоты, они малотоксичны и редко вызывают аллергическую реакцию. Дозы вводимых белковых препаратов зависят от степени нарушения белкового обмена. При компенсированных нарушениях доза вводимого белка – 1 г/кг массы тела в сутки. Декомпенсация белкового обмена, выражающаяся гипопротеинемией, снижением альбумин-глобулинового коэффициента, повышением мочевины в суточной моче, требует введения повышенных доз белка (3–4 г/кг в сутки) и проведения антикатаболической терапии. Сюда включают анаболитические гормоны (ретаболил, нераболил – 25 мг внутримышечно 1 раз в 5–7 дней), построение программы парентерального питания в режиме гипералиментации (140–150 ккал/кг массы в сутки), ингибиторы протеаз (контрикал, трасилол 1000 ЕД/кг в сутки в течение 5–7 дней). Для адекватного усвоения пластического материала каждый грамм вводимого азота необходимо обеспечить 200–220 ккал. Не следует вводить растворы аминокислот с концентрированными растворами глюкозы, так как они образуют токсические смеси. Относительные противопоказания к введению аминокислот: почечная и печеночная недостаточность, шок и гипоксия. Для коррекции жирового обмена и повышения калорийности парентерального питания применяются жировые эмульсии, содержащие полиненасыщенные жирные кислоты. Жир является наиболее калорийным продуктом, однако для его утилизации необходимо выдерживать оптимальные дозы и скорость введения. Жировые эмульсии не должны вводиться вместе с концентрированными полиионными растворами глюкозы, а также перед и вслед за ними. Противопоказания для введения жировых эмульсий: печеночная недостаточность, липемия, гипоксемия, шоковые состояния, тромбогеморрагический синдром, расстройства микроциркуляции, отек мозга, геморрагические диатезы. Необходимые данные основных ингредиентов по парентеральному питанию приведены в таблице 12 и таблице 13. Таблица 12 Дозы, скорость, калораж основных ингредиентов для парентерального питания 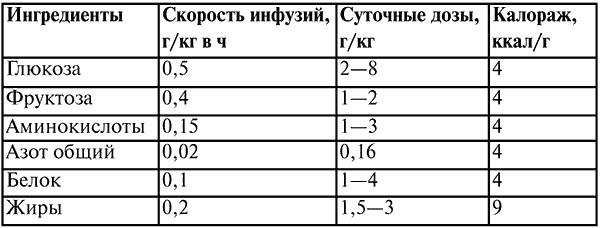 При назначении парентерального питания необходимо вводить оптимальные дозы витаминов, которые участвуют во многих обменных процессах, являясь коферментами в реакциях утилизации энергии. Таблица 13 Дозы витаминов (в мг на 100 ккал), необходимые при проведении парентерального питания 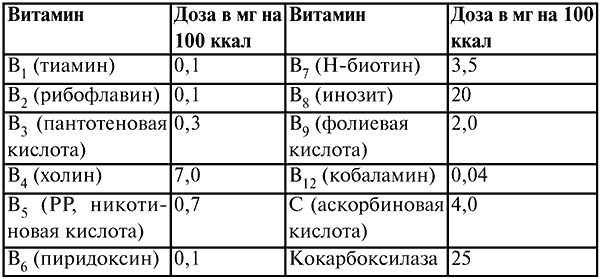 Программа парентерального питания, проводимого в любом режиме, должна быть составлена в условиях сбалансированного соотношения ингредиентов. Оптимальное соотношение белков, жиров, углеводов – 1: 1,8: 5,6. Для расщепления и включения белков, жиров и углеводов в процессе синтеза необходимо определенное количество воды. Соотношение между потребностью в воде и калорийностью пищи составляет 1 мл Н2О – 1 ккал (1: 1). Расчет потребности энергозатраты покоя (ЭЗП) по Харрису– Бенедикту: Мужчины – ЭЗП = 66,5 + 13,7 ? масса, кг + 5 ? рост, см – 6,8 ? возраст (годы). Женщины – ЭЗП = 66,5 + 9,6 ? масса, кг + 1,8 ? рост, см – 4,7 ? возраст (годы). Величина ЭЗП, определенная по формуле Харриса—Бенедикта, составляет в среднем 25 ккал/кг в сут. После проведенного расчета выбирают фактор физической активности больного (ФФА), фактор метаболической активности (ФМА), основанный на клиническом статусе, и температурный фактор (ТФ), с помощью которых будет определена потребность в энергии (ПЭ) конкретного больного. Коэффициент для расчета ФФА, ФМА и ТФ приведены в таблице 14. Таблица 14 Коэффициент для расчета ФФА, ФМА и ТФ  Для определения суточной ПЭ умножают величину ЭЗП на ФФА, на ФМА и на ТФ. 3. Дезинтоксикационная терапия При тяжелых интоксикациях необходима активная дезинтоксикационная терапия, направленная на связывание и выведение токсинов из организма. С этой целью чаще всего используют растворы поливинилпирролидона (неокомпенсан, гемодез) и желатиноль, адсорбирующие и обезвреживающие токсины, которые потом выводятся почками. Эти растворы вводят капельно в количестве 5—10 мл/кг массы больного, добавляя в них витамин С и раствор хлористого калия в минимальном количестве 1 ммоль/кг массы тела. Выраженным дезинтоксикационным свойством обладает также мафусол, являющийся эффективным антигипоксантом и антиоксидантом. Кроме того, он улучшает микроциркуляцию и реологические свойства крови, что также способствует дезинтоксикационному эффекту. При различных отравлениях одним из наиболее эффективных способов дезинтоксикации является форсированный диурез. Внутривенное введение жидкостей с целью проведения форсированного диуреза назначают при тяжелых степенях отравлений и при более легких, когда больной отказывается пить. Противопоказаниями к форсированному диурезу являются: острая сердечно-сосудистая недостаточность и острая почечная недостаточность (анурия). Проведение форсированного диуреза требует строгого учета объема и количественного состава вводимой жидкости, своевременного назначения диуретиков, четкого клинического и биохимического контроля. В качестве основного раствора для водной нагрузки предложено: глюкоза 14,5 г; натрия хлорид 1,2 г; натрия гидрокарбонат 2,0 г; калия хлорид 2,2 г; вода дистиллированная до 1000 мл. Этот раствор изотоничен, содержит необходимое количество гидрокарбоната натрия, концентрация калия в нем не превышает допустимую, а соотношение осмотической концентрации глюкозы и солей равно 2: 1. На начальном этапе форсированного диуреза целесообразно ввести также плазмозамещающие и какие-либо дезинтоксикационные растворы: альбумин 8—10 мл/кг, гемодез или неокомпенсан 15–20 мл/кг, мафусол 8—10 мл/кг, рефортан или инфукол 6–8 мл/кг, реополиглюкин 15–20 мл/кг. Общее количество вводимых растворов ориентировочно должно превышать суточную потребность в 1,5 раза. |
|
||
