|
||||
|
|
35. ОСНОВНЫЕ ТИПЫ ХИМИЧЕСКИХ И МЕЖМОЛЕКУЛЯРНЫХ СВЯЗЕЙ. ИОННАЯ СВЯЗЬ Атомы в молекулах и кристаллах удерживаются почти полностью силами электростатического притяжения между отрицательно заряженными электронами и положительно заряженными ядрами. Роль сил магнитного происхождения весьма незначительна, а гравитационными силами вообще можно пренебречь. Взаимодействие атомов, возникающее в результате частичного или полного обобществления электронов и сопровождающееся уменьшением полной энергии молекул и кристаллов по сравнению с полной энергией их атомов в свободном состоянии, когда атомы удалены друг от друга на бесконечные расстояния, называется химической связью, а разность этих двух энергий – энергией химической связи. Различают следующие основные типы химических связей: 1) ионная, или гетерополярная; 2) ковалентная, или гомеополярная; 3) металлическая. К основным типам межмолекулярных связей относят связь Ван дер Ваальса и водородную связь. Кратко рассмотрим каждый из названных типов связей. Ионная связь обусловлена электростатическим взаимодействием противоположно заряженных ионов. К числу молекул с ионной связью можно отнести хлориды калия, натрия, окисел магния и прочее, а также кристаллы с аналогичным химическим составом. За счет электростатического притяжения ионы сближаются, их внешние электронные оболочки начинают перекрываться (рис. 1), что приводит к возникновению сил отталкивания. 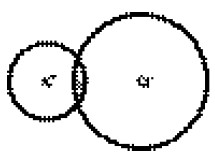 Рис. 1. Область перекрытия ионов K+ и Cl-, аппроксимированных сферами резко ограниченных радиусов в молекуле KCl Отталкивание объясняется взаимодействием электронных оболочек ионов с учетом принципа Паули. Этот тип отталкивания является основным во всех молекулах, кроме самых легких (например, H2). Отталкивание связано также с электростатическим взаимодействием ядер, но для всех молекул, за исключением самых легких, оно не является основным. На некотором расстоянии между ядрами силы притяжения уравновешиваются силами отталкивания, при этом энергия молекулы принимает минимальное значение, что соответствует устойчивому состоянию молекулы. |
|
||
